发布日期:2026-02-09

川贝母作为传统名贵中药材,广泛应用于中成药、保健品等产品中。然而,由于野生川贝母资源稀缺、价格昂贵,市场上掺假现象频发,严重影响产品疗效与市场公信力。更关键的是,川贝母在储存过程中易因条件不当导致DNA降解,传统形态学鉴定、常规PCR等方法难以对降解样本进行准确鉴别,进一步加剧了质量控制的难度。
全球膳食补充剂市场规模预计2028年将突破3000亿美元,中药材作为重要组成部分,其质量安全备受关注。分子鉴定技术因特异性强、准确性高成为中药材鉴别主流方向,但高度降解DNA的检测一直是行业难题。数字PCR(dPCR)作为第三代核酸定量技术,凭借绝对定量能力、高灵敏度及抗干扰性优势,为解决这一痛点提供了技术可能,因此团队开展本研究以建立针对降解川贝母DNA的专属检测方案。
本研究先对比传统DNA编码、迷你编码(mini-barcoding)与巢式PCR技术在降解川贝母DNA检测中的效能,明确传统技术在高度降解样本检测中的局限;进而针对性设计川贝母特异性引物与探针,建立并系统优化dPCR检测体系;最终通过验证该dPCR方法的灵敏度、特异性、定量准确性及临床适用性,实现对高度降解川贝母样本的快速精准鉴定,为解决川贝母因DNA降解导致的真伪鉴别难题提供技术支撑。
研究方法
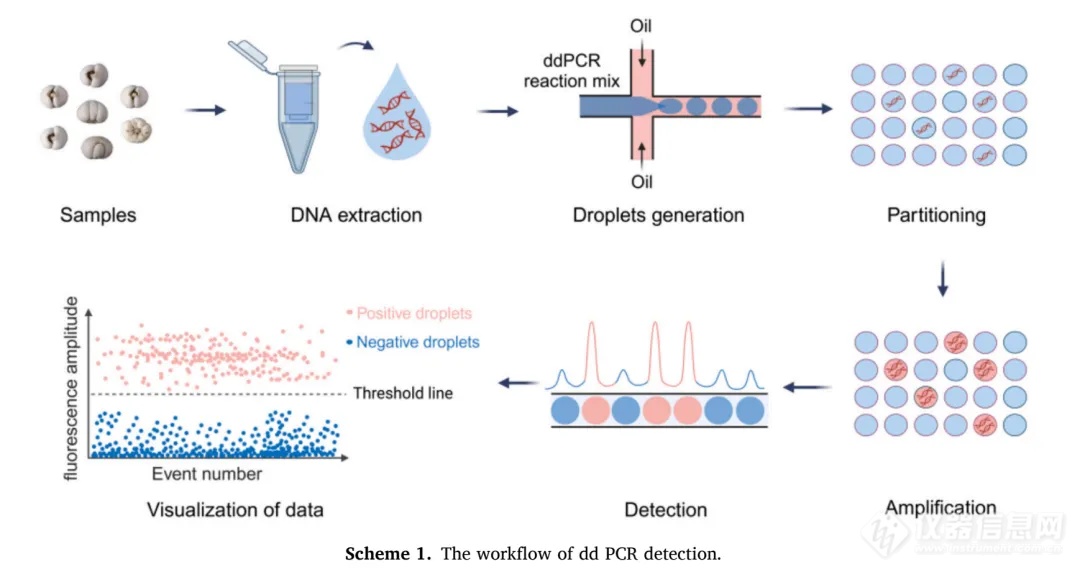
研究结果
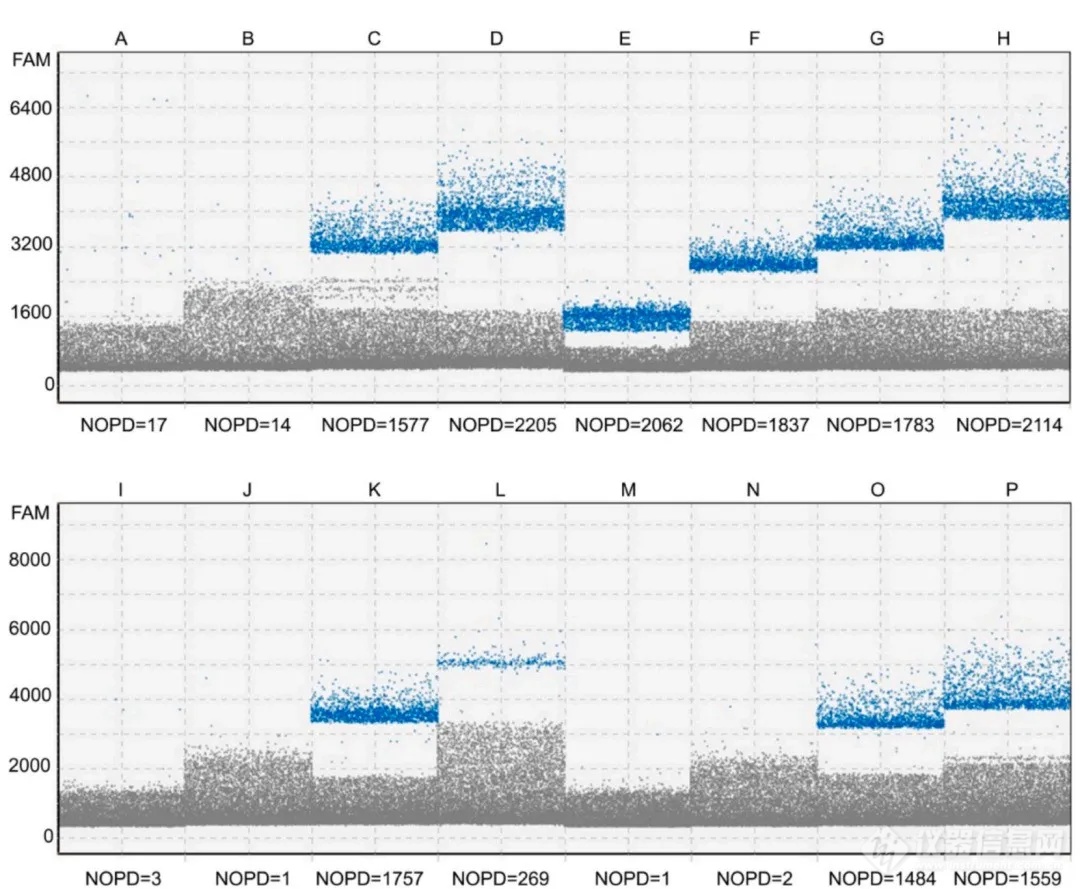
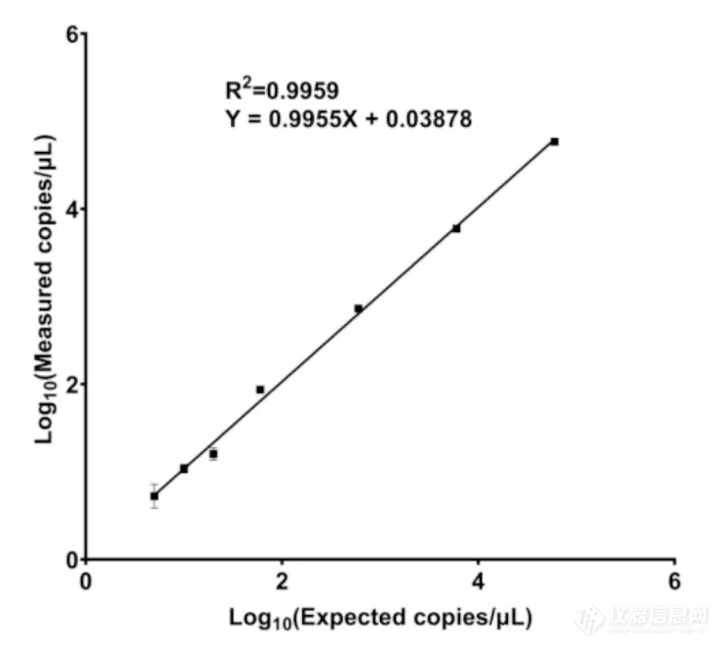
※ 特异性100%,可有效区分掺假物种
对伊犁贝母、平贝母、浙贝母、湖北贝母等常见掺假物种的检测结果均为阴性,仅川贝母样本出现特异性阳性信号,可精准区分正品与掺假品。
※ 样本检测与测序结果100%吻合
dPCR成功检测所有25份样本,其中23份呈现阳性信号(确诊为川贝母),2份无阳性信号,经测序验证分别为伊犁贝母(F. pallidiflora)和平贝母(F. ussuriensis)。即使对于1972年采集的高度降解样本,仍能稳定检出目标DNA,检测全程仅需半天,远快于巢式PCR+测序的1-2天周期。
总结与讨论
该方法的建立,不仅为川贝母的真伪鉴别及质量控制提供了科学有效的技术方案,更为其他易降解中药材(如人参、天麻等)及高度加工膳食补充剂的鉴定提供了重要范式。随着中药材国际化进程加快,dPCR技术有望成为中药材分子鉴定的主流方法,助力规范市场秩序、保障消费者用药安全。
原文链接:
https://doi.org/10.1016/j.microc.2025.116646
●关于新羿生物●
新羿生物成立于2015年,位于中关村科技园,是国家高新技术企业、北京市“专精特新”企业,专注于生命科学与分子诊断的自主创新,拥有在仪器、芯片、材料、试剂、软件等领域的高水平研发团队。公司发展迅速,申请国内外专利200余项、授权专利150余项,持续在权威期刊发表学术论文,承担国家级科研基金。公司基于自主知识产权的数字PCR技术,已获得首个及第二个共三项数字PCR仪NMPA III类医疗器械注册证,三项诊断试剂NMPA III类医疗器械注册证,其中感染和实体瘤液体活检领域均为首个数字PCR诊断试剂III类注册证,两次获得中国体外诊断优秀创新产品金奖,荣获中关村国际前沿科技创新大赛总冠军,荣获北京市科学技术二等奖和发明创业成果奖。公司自主研发的开放式分子POCT一体机及qPCR快检试剂均获NMPA III类医疗器械注册证。公司秉承“创新,让精准触手可及”的理念,发展多指标、高通量、自动化、防污染、成本低的先进技术,致力于成为领先的生命科学和分子诊断企业,服务于生命科学、精准医疗、药物开发及健康管理。

京公网安备 11010802028168号