发布日期:2022-10-27

慢性粒细胞白血病(简称CML)是骨髓造血干细胞克隆性增殖形成的恶性肿瘤,占成人白血病的15%[1],目前全球约有120万-150万慢粒患者。慢粒白血病(CML)的发病原因与费城染色体(Ph)密切相关,大约有95%以上的病人具有费城染色体(Ph),即慢粒患者体内的9号和22号染色体相互易位,产生致癌的BCR-ABL融合基因;因此9月22日被定为“国际慢粒日”。典型的临床表现、体征和(或)血液骨髓细胞检查异常,合并Ph染色体和(或)有BCR/ABL融合基因阳性即可确诊为CML。
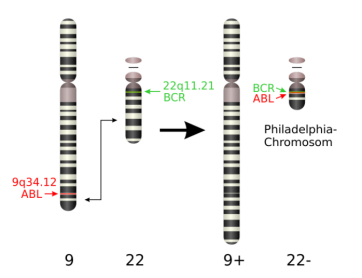
费城染色体易位
慢粒诊疗中的BCR-ABL/ABL突变比值(%IS)监测
CML患者的诊疗全程,包括:疾病类型的鉴别与分层,不同治疗方案的选择,疗效及病程监测,停药时机判断和停药后复发监测等,都需要进行BCR-ABL/ABL突变比值(%IS)的监测。
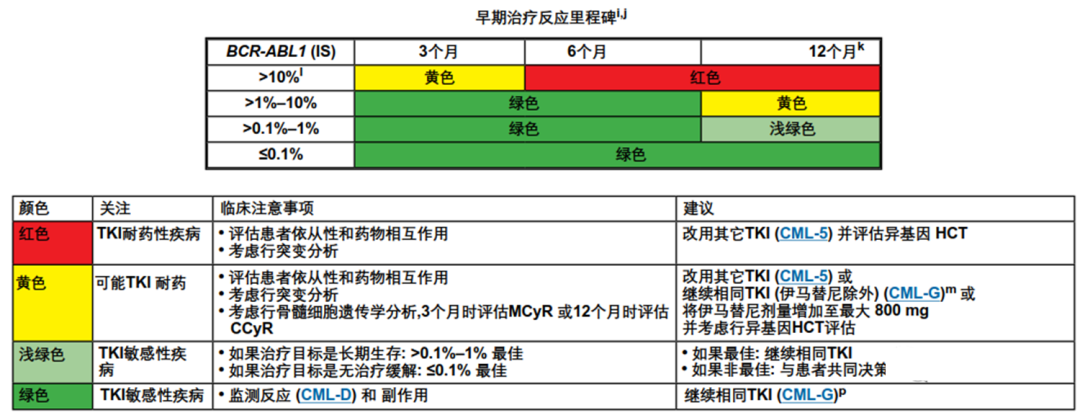
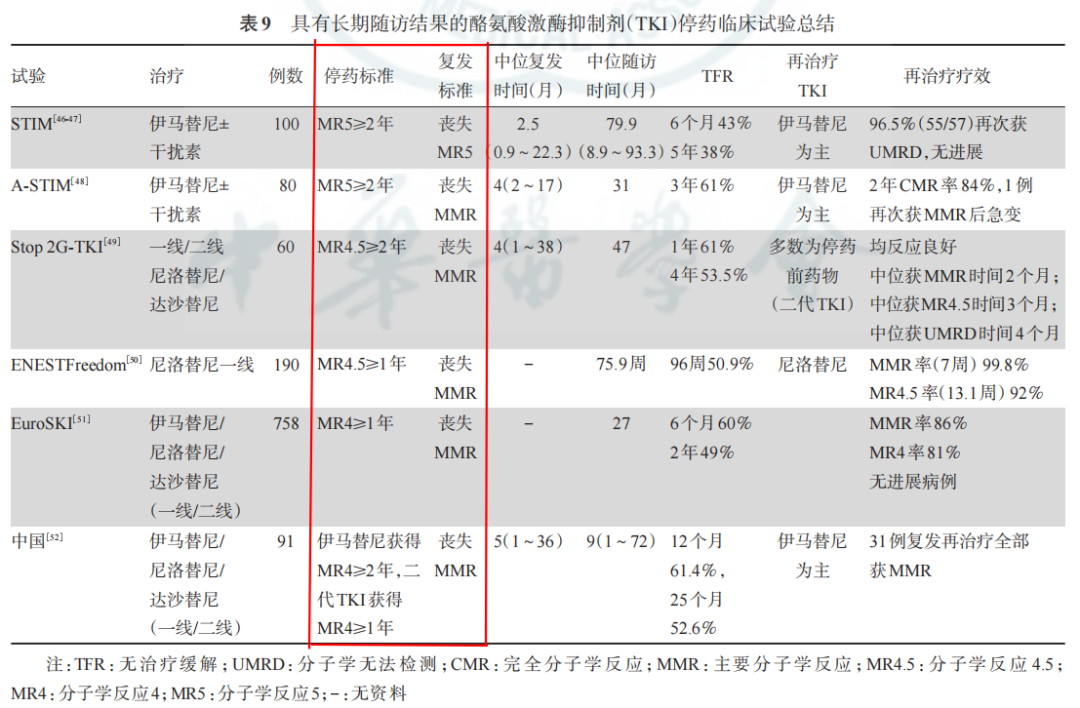
CML中国诊疗指南(2020年版)停药与复发试验总结
Maria Teresa Bochicchio等进行了一项多中心研究,比较dPCR与RT-qPCR检测BCR-ABL%IS的差异,结果表明:dPCR与RT-qPCR检测结果有很好的一致性,但dPCR能更精确地量化BCR-ABL1转录水平,可代替RT-qPCR应用于停药临床试验中[2],如下表所示:
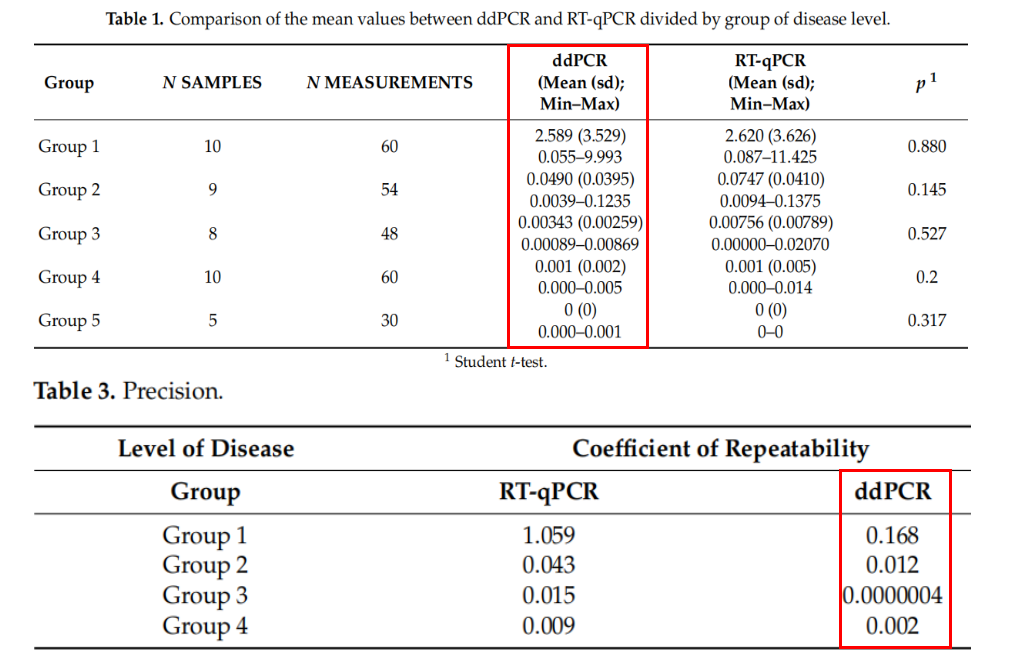
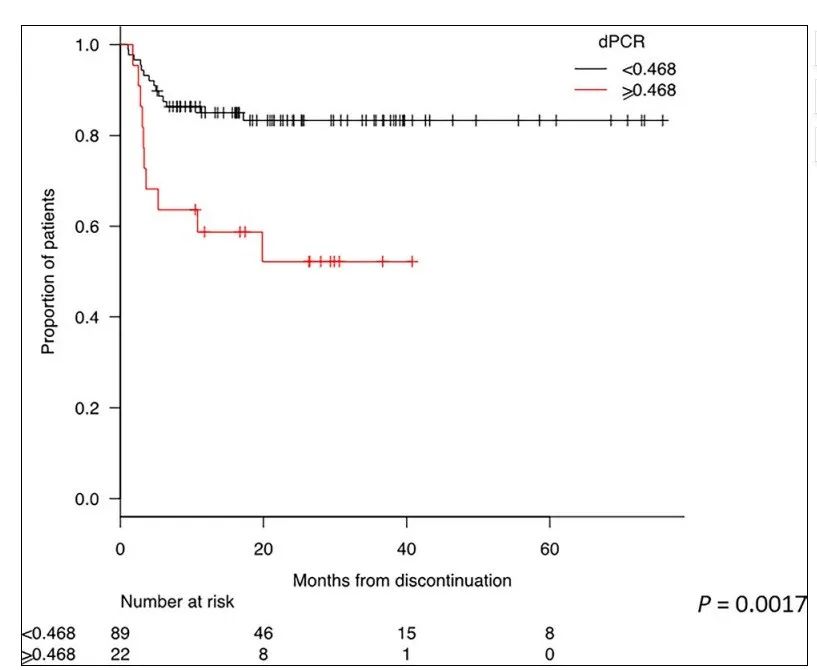
Simona Bernardi等对142例CML患者进行了中位时间为24个月的监测,以比较dPCR和RT-qPCR检测BCR-ABL1转录本的准确性。结果发现:RT-qPCR无法区分停药后MR缺失风险较高的患者(P=0.8100);dPCR检测BCR‐ABL1<0.468 copies/µL的患者较BCR‐ABL1≥0.468 copies/µL的患者,显示出更长的DMR持续时间(P=0.0220),且主要分布在MR4.5‐5.0范围内(P=0.0442);相较于dPCR检测BCR-ABL1值≥0.468 copies/µL的患者,dPCR检测BCR‐ABL1值<0.468 copies/µL的患者终止TKI的无治疗缓解率明显更高(2年TFR分别为83%和52%,P=0.0017);dPCR检测方法可提高DMR稳定性预估和停药时机的把控[3],如下图所示:
新羿BCR-ABL1检测产品
新羿生物自主研发的人白血病融合基因(BCR-ABL1)检测试剂盒(数字PCR法),采用数字PCR方法,定量检测人全血样本中的BCR-ABL融合基因P210 突变型和内源基因ABL表达的RNA拷贝数,计算获得BCR-ABL/ABL的突变比值,指导CML等白血病的诊断和治疗过程,助力停药时机的准确把握和停药后复发的超敏监测。
2021年10月,全国各大血液病非公医疗机构,发起了“血液肿瘤能力提升项目 BCR-ABL1 P210 室间比对活动”,新羿生物“人白血病融合基因(BCR-ABL1)检测试剂盒(数字PCR法)”作为数字PCR 方法的指定试剂,全程深入参与,试剂性能和结果受到各方的肯定和欢迎。此外,新羿生物“人白血病融合基因(BCR-ABL1)检测试剂盒(数字PCR法)”在多家临床单位进行了科研合作,取得了广泛积极的反馈,为该试剂盒的临床应用奠定了坚实的基础。
绝对定量,结果稳定:可实现待检测模板绝对定量,结果受扩增效率等因素影响小。
灵敏度高,应用更广:可检测MR5.0(0.001%IS),适用各种MR水平的样品。
杜绝污染,准确度高:含有dUTP/UNG酶防污染,全程不开盖,实现零污染,保证结果准确。
简单快捷,节省成本:操作简便,样本管数少,节省时间、样本及人工成本。
[1] 中华医学会血液学分会. 慢性髓性白血病中国诊断与治疗指南(2020年版)[J]. 中华血液学杂志, 2020, 41(5): 353-64.
[2] BOCHICCHIO M T, PETITI J, BERCHIALLA P, et al. Droplet Digital PCR for BCR-ABL1 Monitoring in Diagnostic Routine: Ready to Start? [J]. Cancers (Basel), 2021, 13(21):5470.
[3] BERNARDI S, MALAGOLA M, ZANAGLIO C, et al. Digital PCR Improves the Quantitation of DMR and the Selection of CML Candidates to TKIs Discontinuation [J]. Cancer Medicine, 2019, 8(5): 2041-55.

京公网安备 11010802028168号